【研究情報】
今村伸太朗
- 海洋生物の環境適応機構に関する国際シンポジウムが2003年2月22-23日に東京大学で開催されました。筆者らは「Cold sensitive transcriptional mechanism of the zebrafish CDC48 gene (ゼブラフィッシュ細胞分裂周期遺伝子CDC48の低温感受性転写調節機構)」という演題を発表したところ,ベストポスター賞を受賞することができました。環境適応の分野の研究者が招かれたこのようなシンポジウムで私たちの研究が認められたことは本当にうれしく,今後の研究活動を自信をもってやっていけそうです。この3年間,中央水研で学位論文の課題として取り組んだ研究とこのシンポジウムで発表した成果について報告します。
- 魚類は幅広い温度適応能を持っています。この温度適応に関する生物機能は環境水温に強く影響される回遊や行動のパターンを特徴付けています。また,胚や仔稚魚では1℃単位の微妙な温度の差異が生残を決めることから,水産資源の再生産を考え,種苗生産技術を確立する上で特に重要です。さらに,生物が生育してきた温度条件が水産物としての品質を左右することもわかってきました。このように環境水温への適応機構は水産資源,養殖,食品分野など水産全般に関わる重要な研究テーマです。
- 魚種によって遺伝的に異なる温度適応能を持っており,温度条件によって活性化する,あるいは抑制される遺伝子の発現パターンがこのような性質を決めていると考えられました。これまでにも,生理生化学的な研究によって,魚類が高温および低温条件に順化して,魚体の構成成分や生理機能が変化する現象は広く知られています。例えば,低温条件に順化すると誘導されるタンパク質として,乳酸脱水素酵素,アセチルコリンエステラーゼ,ミオシンなどが発見され,その誘導の分子機構も次第に解明されつつあります。また,低温で細胞膜の流動性が失われ,細胞機能が低下するのを補償するため,低温条件では不飽和化酵素が誘導され脂質を不飽和化して膜機能を向上させる現象も見つかっています(1)。
- 魚類から分離された遊離細胞の培養可能な温度条件は,魚類の生育の適温に反映されています。例えば,ニジマス培養細胞は4℃から24℃まで増殖しますが,ニジマスは4℃から22℃まで飼育可能です。細胞レベルでの温度に対する応答と制御が魚類の水温への適性を決めている可能性が考えられました。
- このような背景から,ニジマス培養細胞を4℃で培養すると誘導される細胞分裂周期遺伝子CDC48のホモログが同定されました(2)。この遺伝子は,ATPases associated with diverse cellular activities (AAA)ファミリーに属しており,酵母のCDC48欠損株を使った研究から,細胞分裂に必須の因子として同定されています。最近の研究では細胞分裂後の小胞体膜の再構成や,異常なタンパク質と正常なタンパク質との選別に関わる分子として作用することが推定されています。マウス,ゼノパス,シロイヌナズナ,酵母などからも単離され,生物に共通して分布しています。この遺伝子の低温条件での発現が,魚類細胞の増殖低下を補償していることが考えられました。そこで,低温条件下に細胞が置かれたとき,CDC48遺伝子が誘導される機構と低温下での細胞分裂を促進する機能の解明を目指しました。
- CDC48遺伝子の単離

図1.ゼブラフィッシュ培養細胞におけるCDC48の低温誘導性
30℃から15℃に細胞の培養温度を下げるとCDC48が誘導された.抗CDC48抗体を用いてウエスタンブロット法で検出した.HSC70は内部コントロール.
|
|---|
- 低温条件下でのこの遺伝子の働きを明らかにするために,まず,遺伝子を単離しました。ゼブラフィッシュは約3万個の遺伝子を持つことが推定されていますが,それらのほとんどを含む遺伝子図書館(ゲノムDNAライブラリーおよびcDNAライブラリー)を用いて,リン-32で放射能標識したDNAプローブで目的の魚類DNAを持つ大腸菌クローンをスクリーニングしました。約100万個の大腸菌クローンからCDC48遺伝子のDNAを持つクローンを単離しました。DNAの塩基配列は国際遺伝子データベースに登録しました。
- ゼブラフィッシュは細胞および生体への外来遺伝子の過剰発現 (gain of function)や抑制試験 (loss of function) が可能であり,生体内の遺伝子の発現レベルを改変することにより遺伝子の作用を調べることができます。培養,飼育が容易で,水産分野に限らず,発生生物学,分子遺伝学などのモデル動物として位置づけられています。また,ゼブラフィッシュ由来の培養細胞を用いて,この遺伝子の誘導条件を調べました。この細胞株を30℃から12~25℃に下げるとCDC48遺伝子が誘導され,温度が低いほど強く発現することが明らかになりました(3,4)。このような発現量の変化は培養温度をシフトした後5日目以降に観察され遺伝子産物は1ヶ月ほどかかって徐々に蓄積されていきます。
- CDC48遺伝子の過剰発現による増殖促進作用
- 培養細胞へ目的の遺伝子を導入し,過剰に発現させると細胞内での遺伝子の作用を増強することができます。ゼブラフィッシュ細胞にCDC48遺伝子の発現系を導入したのち,細胞を低温処理すると,低温での細胞の増殖が著しく促進され,この遺伝子が低温下での細胞増殖を促進する作用を持つことが明らかになりました(4)。CDC48遺伝子産物は806残基のアミノ酸からなるポリペプチドですが,細胞内では6量体を構成して1つの分子として働きます。C末端の805残基目に位置するチロシン残基がリン酸化されることによりこの分子の活性が調節されることがわかりました。チロシン残基をアラニン残基に変換した改変遺伝子を作製し,リン酸化を抑制すると,この分子は細胞内で機能することができず,低温条件で細胞増殖を促進するどころか,アポトーシス(細胞死)が生じて細胞数は減少しました。このことからCDC48遺伝子は低温条件で細胞が増殖するために必須の因子であることが明らかになりました。DNA合成能とアポトーシスの発現を調べると,この分子は低温下でDNA合成能を高め,低温で生じるアポトーシスを抑制することがわかりました。マウスや酵母の研究から,CDC48は小胞体に蓄積した異常タンパク質を除去する機能を持つことが推定されています。これらのことから,魚類の培養細胞が低温条件に置かれると,低温のためタンパク合成に異常が生じて異常タンパク質が細胞内に蓄積しますが,CDC48も誘導されて異常タンパク質が除去されることにより,細胞機能が向上することが考えられました。
- CDC48遺伝子の低温誘導性発現機構
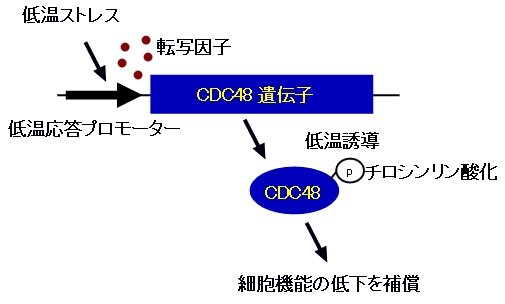
図2.低温条件におけるCDC48遺伝子の発現と細胞内機能
低温ストレスによりCDC48遺伝子上流のプロモーターに転写因子が結合し,転写が活性化される。CDC48はC末端のチロシン残基がリン酸化されることにより活性化され,低温条件で低下した細胞機能が向上する。
|
|---|
- 動物細胞で働く低温誘導性の遺伝子発現機構はこれまで未解明の課題でした。大腸菌や植物から見つかった低温誘導性の遺伝子では,遺伝子の上流域にある調節配列に転写因子が結合し,遺伝子の転写を促進する機構が示されています。魚類における低温誘導性の転写調節機構を明らかにするために,遺伝子上流のプロモーターの転写調節に関わる塩基配列を徹底的に調べました。このプロモーターには,細胞分裂や発生を制御するタンパク質が結合して転写を調節するDNA配列が含まれることがわかりました。このような遺伝子発現の制御に関わるDNA配列(シスエレメント)を同定するために,プロモーターの下流に蛍光タンパク質遺伝子を連結して,魚類胚に導入するとプロモーターの転写能に応じて,強い蛍光を発する細胞を観察することができます。その結果,転写を開始する部分から上流-887~-318 bp の間に転写を活性化するエレメント配列が含まれることがわかりました。細胞の核抽出物とプロモーターのDNAを混合したのち,DNAを分解処理すると転写因子が結合したDNAの配列は分解されずに残ることから,転写因子が結合するエレメント配列を同定することができます。このプロモーターではAATAAA配列を持つ繰り返し構造を介して転写が活性化されていることがわかりました。ここで得られたDNA配列は特許として出願中です。
- CDC48の胚発生での役割
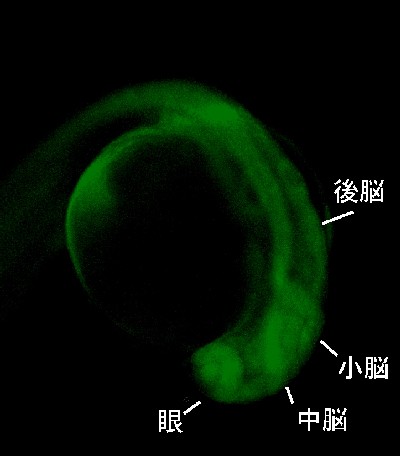
図3.ゼブラフィッシュ胚を用いたプロモーターアッセイ
CDC48プロモーター下流に蛍光タンパク質遺伝子を連結した発現系をゼブラフィッシュ胚に導入し,トランスジェニック系統を作出した.受精後24時間に眼,脳などで強い蛍光が観察された.
|
|---|
- 興味深いことに,CDC48遺伝子の発現レベルは胚発生で急激に増加することがわかりました(5)。ゼブラフィッシュ胚におけるCDC48遺伝子の発現パターンを調べるために,CDC48遺伝子プロモーター下流に蛍光タンパク質遺伝子を連結してゼブラフィッシュ胚に遺伝子導入したところ,受精後16時間(体節形成期)まで蛍光タンパク質の発現が増加し,その後のステージでは発現量は減少に向かいました。特に神経系で強く発現していることがわかりました。培養細胞と胚の両方でプロモーター配列上のエレメント配列を調べると,培養細胞と胚ではそれぞれ異なるエレメント配列が見つかり,低温条件誘導性の遺伝子発現と胚発生のそれとでは転写調節機構が異なっていました。
- 胚発生でのCDC48 遺伝子の役割を明らかにするために,この遺伝子の翻訳を阻害する実験も試みました。CDC48遺伝子のメッセンジャーRNAにハイブリダイズして,特異的に結合する20塩基の短いオリゴDNAアナログ(モルフォリノオリゴDNA)を胚に注入するとCDC48遺伝子のmRNAからのタンパク合成が阻害されます。胚の形態を観察すると,一部の細胞がアポトーシスを生じるため,発生が途中で停止し,斃死することから,この遺伝子が発生に必須の因子であることがわかりました。アポトーシスは特に脳,眼で強く発現していることから,神経系の発生異常が原因であると考えられます。CDC48は脳で生成された異常タンパク質を除去する作用を持つことが推測されていることから,形態形成過程で生じた異常タンパク質の蓄積が生じている可能性があります。

図4.CDC48遺伝子ノックダウンによるゼブラフィッシュ胚の発生異常
CDC48遺伝子に対するモルフォリノオリゴを注入すると,アポトーシスが過剰に発現し,眼が縮小し,脳形成に遅れが見られ,臓器が形成される前に発生が停止した.矢印は形態以上が見られた箇所を示す.下は正常な胚.受精4日後.
|
|---|
- 水産研究におけるさらなる研究の展開
- 魚類の温度適応に関わる分子機構が明らかになってきました。ここで調べてきたCDC48などの遺伝子の誘導レベルを魚体で測定すると,その魚がどのような水温環境に順応しているのかを推定することが可能です。この遺伝子は魚類の低温耐性に関与することがわかりましたが,このような遺伝子機能を向上させることにより,低温に耐性をもつ魚の分子育種が実現するかもしれません。
- 引用文献
| 1. | Hochachka, P. W. and Somero, G. N. (2002) Biochemical Adaptation: Mechanism and Process in Physiological Evolution, Oxford University, Oxford, NY. |
| 2. | Yamashita, M., Ojima, N. and Sakamoto, T. (1996) FEBS Lett. 382, 261-264. |
| 3. | Imamura, S., Ojima, N. and Yamashita, M. (2002) Fish. Sci. 68, 1291-1292. |
| 4. | Imamura, S., Ojima, N. and Yamashita, M. (2003) FEBS Lett. in Press |
| 5. | 今村伸太朗,尾島信彦,山下倫明,平成15年度日本水産学会要旨集,p228. |
(加工流通部加工技術研究室・東京水産大学連携大学院)
Shintarou Imamura
 中央水研ニュース No.32目次へ 中央水研ニュース No.32目次へ
 中央水研ホームページへ 中央水研ホームページへ
|